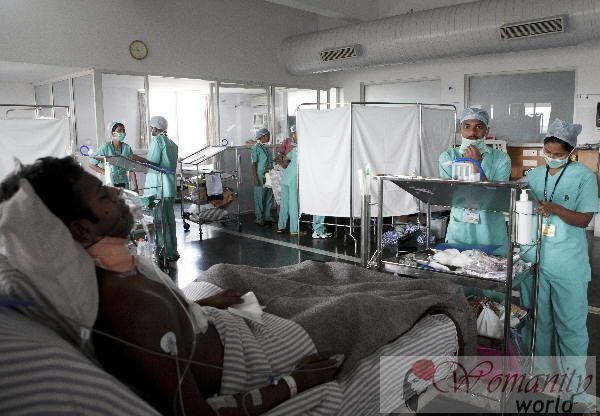
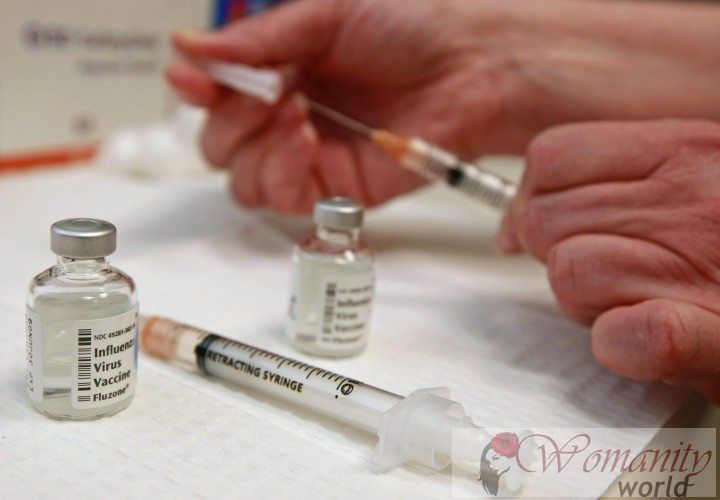
Gli esperti sostengono che l'autorizzazione dei medicinali è accompagnato da un finanziamento
l'autorizzazione anticipata di un medicinale deve essere accompagnato da un finanziamento, come hanno coinciso vari esperti in farmacia nel corso di un seminario, organizzato dalla Fondazione per la ricerca sulla salute (FUINSA) a Madrid, dove hanno esaminato la controversia in questa materia
Altre notizie
- È l'assistenza sanitaria uguale per le donne che per gli uomini?
- Quali sono biologici?
In questo giorno, che è stato intitolato "Early Autorizzazione all'utilizzo di medicinali: prove e di finanziamento", hanno anche affrontato le restrizioni alla determinazione del prezzo dei farmaci innovativi e di rischio per l'accesso dei pazienti.
Il dibattito è stato moderato dal presidente della FUINSA, Alfonso Moreno; CEO, Antón Herreros, e capo di Farmacologia Clinica Ospedale Clinico San Carlos di Madrid, Emilio, Emilio Vargas.
direttore Area di farmacia e medicina Consorzio della Salute sociale della Catalogna, Antoni Gilabert, ha sottolineato che "l'autorizzazione all'inizio dei medicinali deve essere accompagnata da meccanismi espliciti per condizioni di monitoraggio e di finanziamento, e la loro revisione sistematica basata sui risultati. "
Questo esperto ha proposto che i forum di discussione generano abbastanza per rispondere a questa domanda: "Come faremo a pagare per questi nuovi farmaci?".
Farmaindustria direttore tecnico, Emili Esteve, ha sostenuto che "mettere ostacoli al finanziamento di questi farmaci è ben lungi dall'essere l'intenzione del legislatore europeo."
"Per permettere ai pazienti l'accesso a questi farmaci, mentre decidere sui prezzi e di rimborso dovrebbe essere considerato l'assegnazione di un prezzo provvisorio e rivedibile una volta che le condizioni di finanziamento finali sono decisi", ha aggiunto Esteve.
liberazione anticipata di farmaci "ha messo sul mercato i farmaci con poche prove sulla loro efficacia e sicurezza ed i costi insostenibile per i pazienti e sistemi sanitari" ha assicurato farmacologo clinico Carcas Antonio La Paz ospedale.

Questi farmaci liberazione anticipata, nonostante il suo record, in molti condizionata da parte dell'Agenzia europea per i medicinali e l'Agenzia spagnola per medicinali e prodotti sanitari (AEMPS) volte, mettere in dubbio le prove presentate e sulla adeguatezza del loro finanziamento da parte del sistema Sanitario nazionale, come è stato evidenziato nel corso del dibattito.
Tuttavia, il rappresentante del AEMPS Jorge Camarero ha sottolineato: "Abbiamo bisogno di studi iniziali, ci sono momenti in cui i farmaci sono così promettenti che non possiamo perdere 15 anni deve essere rafforzata; se risulta che aumenterà l'aspettativa di vita e la qualità deve venire prima che il paziente".
I relatori hanno convenuto che le prove sufficienti, una volta autorizzati la droga sono fatte, per la validità esterna oggettivamente, e hanno sostenuto una sorveglianza intensiva post-marketing per confermare l'efficacia e la sicurezza come l'uso frullata questi farmaci.
Il capo di Ematologia e l'Ospedale Clinico San Carlos hemoterapia, Rafael Martínez, ha detto che il più importante per un farmaco ad essere approvato per la dispensa "è quello di migliorare le aspettative dei nostri pazienti".